Wissenschaftliche Hintergründe zur stammzellbasierten Therapie
Bioregenerative Therapie von degenerativen Veränderungen an Gelenken
Der degenerative Verschleiß von Gelenken und die daraus entstehenden Beschwerden und Funktionseinschränkungen für den Patienten stellen nach wie vor eine Herausforderung in der Orthopädie dar, da das Selbstheilungspotential des Körpers – insbesondere im Bereich des schlecht durchbluteten Gelenkknorpels – ohne Unterstützung von außen sehr begrenzt ist.
Aus der Erkenntnis heraus, dass die Unterstützung mit Wachstumsfaktoren notwendig ist, um einen Verschleiß der Gelenke zu stoppen und eine Beschwerdebesserung zu erreichen, hat sich der Einsatz von körpereigenen, biologischen Therapieformen zur Behandlung von Erkrankungen der Gelenke, Bänder, Sehnen oder der Muskulatur im Bereich der Extremitäten oder der Wirbelsäule durchgesetzt und wird inzwischen in Fachkreisen als Goldstandard angesehen. Zuletzt wurde dieser Therapieansatz im Frühjahr 2023 durch den Konsens des orthopädischen Berufsverbandes ESSKA (Europ. Society of Sports Traumatology, Knee Surgery and Arthroscopy) untermauert.
Stammzellen als potente Heiler im Körper
Stammzellen stellen im Körper die potenteste Quelle für derartige regenerative Botenstoffe dar. Die mesenchymalen Stammzellen als Vorläufer unter anderem des Knorpels bieten eine hohe Konzentration an relevanten Wachstumsfaktoren und stehen daher im Fokus der Therapie. Diese mesenchymalen Stammzellen sind in höchster Konzentration im Unterhautfettgewebe des Bauches oder der Oberschenkel zu finden. Dort können sie in örtlicher Betäubung komplikationslos mechanisch gewonnen werden. Anschließend wird die stammzellhaltige Fraktion (stromavaskuläre Fraktion; SVF) gewonnen, indem unter anderem die ölige Phase des Fetts und flüssige Bestandteile durch Zentrifugation abgetrennt werden. Diese rein autologe, also ohne chemische Zusätze entstandene stammzellhaltige Fraktion wird anschließend in das Gelenk injiziert.
Ausdrücklich weisen wir darauf hin, dass in diesem Beitrag der weltweite wissenschaftliche Erkenntnisstand zur stammzellbasierten Therapie der Arthrose dargestellt wird.
In Deutschland ist ausschließlich der Einsatz zur auffüllenden mechanischen Schutz- und Dämpfungsfunktion des Fettkörpers innerhalb des Gelenkes erlaubt. Wir erklären Ihnen die Unterschiede gern im persönlichen Gespräch.
Ist die stammzellbasierte Therapie bei Arthrose wissenschaftlich untersucht?
Zur Erklärung von medizinischen Fachausdrücken halten Sie die Maus über dem entsprechenden Wort. Es wird automatisch eine kurze Erläuterung eingeblendet.
Es wurden bereits zahlreiche Studien zur Behandlung der Arthrose mit einer stromavaskulären Fraktion veröffentlicht. Seit einigen Jahren werden immer mehr Studien auch zu klinischen Ergebnissen publiziert. Wenn man in der Medizindatenbank Pubmed nach den Begriffen „Arthrose“ in Zusammenhang mit „mesenchymalen Stammzellen“ sucht, werden fast 2.400 Treffer gelistet. Dabei nahm die Anzahl der Studien seit 2013 sprunghaft zu.
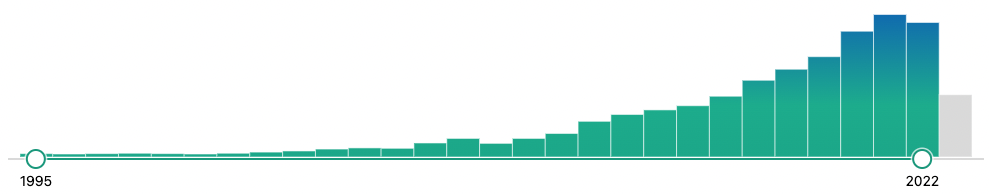
Stammzellbasierte Therapie – Veröffentlichungen in Pubmed von 1995 bis 2022
Die aktuellste Studie aus Deutschland stammt aus dem Jahr 2022. In der Veröffentlichung aus der Forschungsgruppe um Prof. Gerald Zimmermann wurden 33 Patienten mit Gonarthrose durch eine Infiltration der stromavaskulären Fraktion in den Hoffa-Fettkörper therapiert. Nach 6 Monaten konnte eine signifikante Verbesserung der Schmerzen auf der und der entsprechenden Unterskalen des im Vergleich zum Ausgangswert festgestellt werden.
Nach einem Jahr Nachbeobachtung wurde immer noch eine signifikante Verbesserung in allen KOOS-Subskalen im Vergleich zum Ausgangswert festgestellt.
Zusätzlich wurde eine Bestimmung der Zellzahl und der Vitalität der Stammzellen durchgeführt. Es zeigt sich, dass die klinische Verbesserung der Gonarthrose direkt mit der Vitalität und der Anzahl der Zellen korreliert. Das in Deutschland verwendete Verfahren mit rein mechanischer Aufarbeitung garantiert durch die sehr kurze Zeitspanne zwischen Entnahme und Injektion sowie durch die rein mechanische statt enzymatische Aufarbeitung eine hohe Vitalitätsquote bei den Zellen.
Entsteht bei der Behandlung wieder neuer Knorpel?
In einer aus dem Jahr 2023 von Kim und Kollegen wurden 5 analysiert.
Zu den beiden Nachuntersuchungs-Terminen nach 6 Monaten und 12 Monaten wurde in allen Studien eine signifikante Schmerzlinderung sowie eine signifikante funktionelle Verbesserung festgestellt, ohne dass es einen Unterschied bei verfahrensbedingten Knieschmerzen oder Schwellungen im Vergleich zu den Kontrollgruppen gab.
Besonders bemerkenswert in diesem Artikel ist die Erkenntnis, dass in 3 Studien in der MRT-Bewertung ein signifikant verbesserter Knorpelzustand gefunden wurde. Es gibt also Hinweise darauf, dass nicht nur das Fortschreiten der Arthrose gehemmt und die Beschwerden reduziert werden können, sondern dass tatsächlich die Substanz des Knorpels verbessert werden kann.
In einer australischen Studie aus 2019 beurteilte die Forschungsgruppe um Julien Freitag den Kniegelenksknorpel der Patienten nach einer Therapie mit mesenchymalen Stammzellen im MRT. Auch hier zeigte sich, dass das Knorpelvolumen nach der Therapie zugenommen hatte.
Wenn diese Erkenntnisse in weiteren Studien untermauert werden können, wäre das ein Meilenstein in der Arthrosetherapie.
Wie sicher ist die Therapie?
Konrad Slynarski veröffentliche 2017 seine 2-Jahres-Ergebnisse nach stammzellbasierter Therapie am Knie. Die eingeschlossenen 96 Patienten litten an Gonarthrose bis Grad 3 (von vier). Keiner der Patienten hatte in den 12 Monaten zuvor eine Infiltration ins Knie bekommen, es wurde keine gelenkverändernde Operation in der Vergangenheit durchgeführt. Alle erhielten eine einmalige Infiltration mit SVF in Kombination mit Platelet rich plasma.
Nach 2 Jahren hatten sich bei den Patienten sowohl Schmerz (im bereits oben erwähnten ) als auch Funktion (Testinstrumentarium ) signifikant verbessert. Es traten im Lauf der Behandlung keine Komplikationen auf. Diese sehr gute Verträglichkeit und niedrige Komplikationsrate deckt sich auch mit den Ergebnissen anderen Studien (u.a. Kim 2023; Prodromos 2021).
In der Studie von Chadwick Prodromos und Tobias Rumschlag, veröffentlicht 2021, wurden bei insgesamt 2.011 eingeschlossenen Infiltrationen von Stammzellen in Gelenke kein einziges stammzellspezifisches unerwünschtes Ereignis festgestellt. Die stammzellbasierte Therapie ist somit extrem sicher und birgt kein erhöhtes Risiko im Vergleich zu anderen herkömmlichen Behandlungen der Arthritis.
Wie oft muss man die Therapie durchführen lassen?
2020 wurde von Garza und Kollegen eine veröffentlicht, bei der 39 Patienten mit Knieschmerzen eingeschlossen wurden. Sechs Monate nach Therapie hatten die Patienten in der Verum-Gruppe eine 84%ige Verbesserung im gegenüber den Patienten, die nur ein Placebo ins Knie injiziert bekommen haben (25% Besserung in der Placebogruppe). Die Autoren schlussfolgerten, dass mit einer einmaligen SVF-Injektion die Symptome der Gonarthrose, insbesondere der Schmerz, für mindestens 12 Monate signifikant verbessert werden können.
Im Expertenkonsens wird derzeit empfohlen, die Therapie zunächst einmalig anzuwenden. Sollte sich nach ca. 3 Monaten noch nicht der gewünschte Effekt eingestellt haben, kann einmalig eine Injektion mit Plättchenreichem Plasma (ACP) erfolgen.
Eine Wiederholung der stammzellbasierten Therapie ist jederzeit möglich, eine Einschränkung gibt es hier nicht. Sinnvoll ist die Wiederholung aber vermutlich frühestens nach 12 Monaten.
Kann man den Knorpel nicht besser operativ aufbauen?
In einem Review aus 2017 wurden von Weilong und Kollegen 33 Studien ausgewertet, bei denen orthobiologische Therapieoptionen zum Einsatz kamen. Es zeigte sich unter anderem, dass der Einsatz von SVF im klinischen Outcome gleich gut abschneidet wie die deutlich invasivere, belastendere und kostenintensivere matrixassoziierte Knorpeltransplantation (MACI-ACT). Gegenüber dem Einsatz von PRPs kann eine signifikante höhere Verbesserung des Gelenkzustandes erreicht werden.
Bei degenerativem Knorpelverlust, also der klassischen Arthrose, sollte generell keine operative Knorpeltransplantation durchgeführt werden. Falls konservative Verfahren hier nicht mehr ausreichend sind, sollte der künstliche Gelenkersatz (Oberflächenersatzprothese) diskutiert werden.
Zusammenfassung
In allen aufgeführten Studien wurde festgehalten, dass die stammzellbasierte Therapie bei Arthrose – nicht nur im Vergleich mit operativen Verfahren – eine äußerst komplikationsarme und für den Patienten sehr gut verträgliche Therapie ohne größere Einschränkungen darstellt. Gleichzeitig birgt die Therapie ein sehr hohes Potential zur Verbesserung der durch die Arthrose ausgelösten Beschwerden und Einschränkungen.
Wie immer sind bei neuen Behandlungsmethoden in der Medizin noch viele weitere Studien notwendig, um die Vorgänge rund um die stammzellbasierte Therapie zu verstehen.
Im Artikel zitierte Literatur
Zimmermann G et al: Infiltration of the Hoffa’s fat pad with stromal vascular fraction in patients with osteoarthritis of the knee -Results after one year of follow-up. Bone Reports 2022; 16
Kim JH et al: Intra-articular Injection of Autologous M Adipose-Derived Stem Cells or Stromal Vascular Fractions: Are They Effective for Patients With Knee Osteoarthritis? Clinical Sports Medicine Update 2023; 51:837-848
Freitag, J et al: Adipose-derived mesenchymal stem cell therapy in the treatment of knee osteoarthritis: a randomized controlled trial. Regen. Med. 2019, 14 (3), 213–230
Slynarski K et al: Treatment of Osteoarthritis: Adipose Derived Stem Cell and PRP Therapy. Sportärztezeitung. 2017;3:14-18
Prodromos C et al.: Administration of Autologous Mesenchymal Cells for the Treatment of Arthritis. Current Stem Cell Reasearch & Therapy, 2021, 16, 1-8
Garza JR et al: Clinical Efficacy of Intra-articular Mesenchymal Stromal Cells
for the Treatment of Knee Osteoarthritis. The American Journal of Sports Medicine 2020;48(3):588–598
Weilong J et al: Biologic injections for osteoarthritis and articular cartilage damage: can we modify disease? The Physician and Sportsmedicin 2017; Vol. 45,No.3,203–223
Weiterführende Literatur
Zuk PA et al: Human adipose tissue is a source of multipotent stem cells. Molecular Biology of the Cell, 2002;13(12):4279-95
Puissant B et al: Immunomodulatory effect of human adipose tissue-derived adult stem cells: comparison with bone marrow mesenchymal stem cells. Br J Haematol. 2005:129:118-29
Yoshimura K et al: Characterization of freshly isolated and cultured cells derived from the fatty and fluid portions of liposuction aspirates. Journal of Cellular Physiology. 2006;208(1):64-76
Kilroy GE et al: Cytokine profile of human adipose-derived stem cells: expression of angiogenic, hematopoietic, and pro-inflammatory factors. J Cell Physiol, 2007;212(3);702-9
Chen Yet al: Mesenchymal stem cells: a promising candidate in regenerative medicine. Int J Biochem Cell Biol, 2008;40(5):815-20
Conese M et al: Paracrine effects and heterogenity of marrow-derived stem/progenitor cells: relevance for the treatment of respiratory diseases. Cells Tissues Organs, 2013;197(6):445-73
Van Pham Pet al: Activated platelet-rich plasma improves adipose-derived stem cell transplantation efficiency in injured articular cartilage. Stem Cell Research & Therapy, 2013:4(4):91
Koh YG et al: Comparative outcomes of open-wedge high tibial osteotomy with platelet-rich plasma alone or in combination with mesenchymal stem cell treatment: a prospective study. Arthroscopy, 2014;30(11):1453-60
Kasir R et al: Regenerative Engineering of Cartilage using Adipose-Derived Stem Cells. Regen Eng TransI Med, 2015;1(1):42-49
Xu FT et al: Effect of activated autologous platelet-rich plasma on proliferation and osteogenic differentiation of human adipose-derived stem cells in vitro Am J Trans Res, 2015;7(2):257-70
Shen J et al: Autologous platelet-rich plasma promotes proliferation and chondrogenic differentiation of adipose-derived stem cells. Molecular Medicine Reports, 2015;11(2):1298-303
Loibl M et al: The effect of leukocyte-reduced platelet-rich plasma on the proliferation of autologous adipose-tissue derived mesenchymal stem cells. Clin Hemorheol Microcirc, 2016;61(4):599-614
Stessuk T et al: Platelet-rich plasma (PRP) and adipose-derived mesenchymal stem cells: stimulatory effects on proliferation and migration of fibroblasts and keratinocytes in vitro. Arch Dermatol Res, 2016;308(7):511-20
Michalek J et al: Autologous adipose tissue-derived stromal vascular fraction cells application in patients with osteoarthritis. Cell Transplant, 2015 online
Pers YM et al: Adipose Mesenchymal Stromal Cell-Based Therapy for Severe Osteoarthritis of the Knee: A Phase I Dose-Escalation Trial. 2016;5 (7):847-56
Pers YM et al: Adipose derived stem cells for regenerative therapy in osteoarticular diseases.
Horm Mol Biol Clini Invest, 2016;28(3):113-120
Luz-Crawford P et al: Mesenchymal stem cell derived Interleukin 1 rezeptor antagonist promotes macrophage polarization and inhibits B cell differentiation. Stem Cells 2016,34:483-92.
Koh YG et al: Adipose-Derived Mesenchymal Stem Cells with Microfracture versus Microfracture alone: 2-Year Follow-up of a Prospective Randomized Trial. Arthroscopy, 2016:32(1):97-109
Nguyen PD et al: Comparative Clinical Observation of Arthroscopic Microfracture in the Presence and Absence of a Stromal Vascular Fraction Injection for Osteoarthritis. Stem Cells Trans Med, 2016;5:1-9
